ОбЙИарЄСе ЕЭЙЗеш 3 ЧбЎЈбЁУКЭЙ ЮврКЭУь
ЧбЏЈбЁУКЭУьЙ-ЮврКЭУь (Born-Haber Cycle)
ЁУаКЧЙЁвУЗешЛУаЁЭКДщЧТЂбщЙЕЭЙТшЭТ ц ЫХвТЂбщЙЕЭЙ ЗеСеЗбщЇЄвТЄЧвСУщЭЙсХаДйДЄЧвСУщЭЙ рЊшЙ
ЁУаКЧЙЁвУрЁдДтЋрДеТСЄХЭфУДь
(NaCl)
тДТрУдшСЕщЙЈвЁтХЫатЋрДеТСЗешТбЇрЛчЙЂЭЇсЂчЇ (solid ,s) ЫУзЭ
Na(s) сХарУдшСЈвЁЁъвЋЄХЭУеЙ (Cl2) ЫУзЭ Cl2(g) ЋжшЇСеЪСКбЕдрЛчЙтСрХЁиХ ЈаЛУаЁЭКДщЧТЂбщЙЕЭЙТшЭТ
ц ДбЇЙещ
1. тХЫатЋрДеТСЋжшЇрЛчЙЂЭЇсЂчЇфДщУбКЄЧвСУщЭЙрЁдДЁвУЫХЭСрЫХЧ уЫщЄЧвСУщЭЙЕшЭфЛЈЙрДзЭДсХа
ЁХвТрЛчЙфЭ
ЖщвЄдДУЧСЁбЙрЛчЙЂбщЙЕЭЙрДеТЧ ЄзЭЈвЁЂЭЇсЂчЇрЛчЙфЭ (ЁъвЋ) рОзшЭфСшуЫщСеЂбщЙЕЭЙСвЁ
рЁдЙфЛ ЈарЛчЙЁвУУарЫдД рЛчЙЁУаКЧЙЁвУДйДЄЧвСУщЭЙ ДбЇЪСЁвУ ;
Na(s) → Na(g)
; ΔH1
= +107 kJ/mol
2. ЭаЕЭСЂЭЇ Na уЙЪЖвЙаЁъвЋ , Na(g)
фДщУбКОХбЇЇвЙЈЙрЪеТЭдрХчЁЕУЭЙ (ОХбЇЇвЙфЭЭЭфЙрЋЊбЙ
ЭбЙДбК 1 , IE1) ЂбщЙЕЭЙЙещ
рЛчЙЁУаКЧЙЁвУДйДЄЧвСУщЭЙ ДбЇЪСЁвУ
Na(g) → Na+(g) + e- ; ΔH2 = + 496
kJ/mol
3. тСрХЁиХЂЭЇЁъвЋЄХЭУеЙ (Cl2) рЁдДЁвУсТЁЪХвТЭЭЁрЛчЙЭаЕЭСЭдЪУауЙЪРвЧаЁъвЋ рЛчЙЁвУЪХвТ
ОбЙИаУаЫЧшвЇЭаЕЭСЂЭЇЄХЭУеЙуЙтСрХЁиХ ЂбщЙЕЭЙЙещрЛчЙЁУаКЧЙЁвУДйДЄЧвСУщЭЙ ДбЇЪСЁвУ
Cl2(g) → Cl(g)
; ΔH3 = +122 kJ/mol
4. ЭаЕЭСЂЭЇ Cl уЙЪРвЧаЁъвЋУбКЭдрХчЁЕУЭЙ ЁХвТрЛчЙфЭЭЭЙХК ЁУаКЧЙЁвУЙещЄвТОХбЇЇвЙ ЄзЭ
ОХбЇЇвЙЭдрХчЁЕУЭЙЭбППдЙдЕе , EA ДбЇЪСЁвУ
Cl(g) + e- → Cl-(g) ; ΔH4 = -349
kJ/mol
5. Na+(g) УЧСЕбЧЁбК Cl-(g) сХщЧрЛХешТЙЪЖвЙарЛчЙЂЭЇсЂчЇЄзЭМХжЁЂЭЇ
NaCl ЂбщЙЕЭЙЙещЄвТОХбЇЇвЙ
рУеТЁЧшвОХбЇЇвЙтЄУЇУшвЇМХжЁ (lattice energy)
ДбЇЪСЁвУ
Na+(g) + Cl-(g) → NaCl(s)
; ΔH5 =
-787 kJ/mol
ЖщвЙгОХбЇЇвЙЗешрЁешТЧЂщЭЇЁбКЂбщЙЕЭЙЗбщЇ 5 ЂбщЙЕЭЙЙещСвУЧСЁбЙ (ЙгрЄУзшЭЇЫСвТ + ЫУзЭ – ЂЭЇ
сЕшХаЄшвСвДщЧТ) МХХбОЗьЗешфДщрУврУеТЁЧшв
ОХбЇЇвЙЂЭЇЛЏдЁдУдТв (ΔHf) ДбЇЪСЁвУ
ΔHf = ΔH1
+ ΔH2
+ ΔH3 + ΔH4 + ΔH5
= +107 kJ/mol + 122 kJ/mol + 496 kJ/mol
+(-349 kJ/mol) + (-787 kJ/mol)
=
- 411 kJ/mol
рЂеТЙсЪДЇуЙУйЛЪСЁвУУЧСфДщДбЇЙещ
Na(s) + Cl2(g) →
NaCl(s) ; ΔHf =
-411 kJ/mol
уЙЁвУЄгЙЧГОХбЇЇвЙЂЭЇЁУаКЧЙЁвУЕшвЇ
ц ЗгфДщЫХвТЧдИе ЂжщЙЭТйшЁбКЄЧвСрЂщвуЈсХаЄЧвСЖЙбДЂЭЇсЕшХаЄ Й
сЕшЕщЭЇЭТйшКЙЫХбЁЁвУрДеТЧЁбЙЄзЭ
ЕщЭЇУйщЧшвОХбЇЇвЙЪшЧЙЗешДйДрЂщвфЛуЙсЕшХаЂбщЙЕЭЙУЧСЁбЙфДщрЗшвфУ
УйщЧшвОХбЇЇвЙЪшЧЙЗешЄвТЭЭЁСвуЙсЕшХаЂбщЙЕЭЙУЧСЁбЙфДщрЗшвфУ ЙгОХбЇЇвЙ
2 ЪшЧЙЙещСврЛУеТКрЗеТКЁбЙ
ЖщвОХбЇЇвЙЗешДйДрЂщвфЛ СеСвЁЁЧшвЗешЄвТЭЭЁСв ЁУаКЧЙЁвУЙбщЙрЛчЙЁУаКЧЙЁвУДйДЄЧвСУщЭЙ (endothermic process)
; ΔH
уЊщрЄУзшЭЇЫСвТ +
ЖщвОХбЇЇвЙЗешЄвТЭЭЁСв
СеСвЁЁЧшвЗешДйДрЂщвфЛ
ЁУаКЧЙЁвУЙбщЙрЛчЙЁУаКЧЙЁвУЄвТЄЧвСУщЭЙ (exothermic
process) ; ΔH уЊщрЄУзшЭЇЫСвТ -
уЙЁвУрЁдД NaCl ЈгЙЧЙ 1 тСХ (58.5 ЁУбС) ДбЇЕбЧЭТшвЇЖщвЙгЄЧвСУщЭЙЪшЧЙЗешДйДрЂщвфЛуЙсЕшХаЂбщЙЕЭЙСвУЧСЁбЙЈафДщДбЇЙещ
Na(s) → Na(g)
; ΔH1
= +107 kJ/mol
Na(g) → Na+(g) + e- ; ΔH2 =
+ 496 kJ/mol
Cl2(g) → Cl(g)
; ΔH3
= +122 kJ/mol
УЧСОХбЇЇвЙЄЧвСУщЭЙЗешДйД ; = +107 + 496 + 122 = 725 kJ/mol
уЙЗгЙЭЇрДеТЧЁбЙЖщвЙгЄЧвСУщЭЙЪшЧЙЗешЄвТЭЭЁфЛуЙсЕшХаЂбщЙЕЭЙСвУЧСЁбЙЈафДщДбЇЙещ
Cl(g) + e- → Cl-(g) ; ΔH4 = -349
kJ/mol
Na+(g)
+ Cl-(g) →
NaCl(s) ; ΔH5 =
-787 kJ/mol
УЧСОХбЇЇвЙЄЧвСУщЭЙЗешЄвТ ; ΔH2 -349 + (-787) = - 1136 kJ/mol
рСзшЭрЛУеТКрЗеТКУаЫЧшвЇОХбЇЇвЙЪшЧЙЗешДйДЁбКЄвТЈарЫчЙфДщЧшв ЪшЧЙЗешЄвТСеСвЁЁЧшв ЉаЙбщЙЁУаКЧЙЁвУЙещЈжЇрЛчЙсККЄвТЄЧвСУщЭЙ ; ΔHf
= ΔH1 + ΔH2
= + 725 kJ/mol + ( -1136 kJ/mol )
= -411
kJ/mol
ЛЏдЁдУдТвЙещЈаСеЁвУЄвТОХбЇЇвЙЭЭЁСв 411 kJ/mol рСзшЭСе NaCl ЗешрЁдДЂжщЙ 1 тСХ сЕшЖщвСе NaCl рЁдДЂжщЙСвЁЫУзЭЙщЭТЁЧшвЙещ ЁвУЄвТОХбЇЇвЙЁчЈасЛУМбЙЕУЇЁбКЈгЙЧЙтСХЂЭЇ NaCl ЗешрЁдДЂжщЙ
ЖщвЙгЂбщЙЕЭЙЕшвЇ ц
СврЂеТЙсЪДЇрЛчЙсМЙМбЇЕвСХгДбК ЈарУеТЁЧшв Born Haber
Cycle ЫУзЭЧбЏЈбЁУЂЭЇКЭЙ ЮвУьрКЭУь ЉаЙбщЙЧбЏЈбЁУЂЭЇКЭЙ
ЮвУьрКЭУьЈжЇрЛчЙсМЙМбЇсЪДЇЂбщЙЕЭЙЂЭЇЁвУЁвУрЁдДЛЏдЁдУдТвсХаЁвУрЛХешТЙсЛХЇОХбЇЇвЙуЙсЕшХаЂбщЙ ДбЇЙещ

УйЛсККуЙЁвУрЂеТЙсЪДЇЧбЏЈбЁУЂЭЇКЭЙ
ЮвУьрКЭУь
фСшфДщЁгЫЙДУйЛсККЕвТЕбЧ
ЄЧвСЪгЄбЭТйшЗешЄЧвСЕшЭрЙзшЭЇЂЭЇЂбщЙЕЭЙ
сХасЪДЇОХбЇЇвЙЗешрЁешТЧЂщЭЇуЫщЕУЇЁбЙ
рЊшЙ ЧбЏЈбЁУЂЭЇКЭЙ ЮвУьрКЭУьсЪДЇЁвУрЁдД LiF
ЪвСвУЖрЂеТЙфДщЫХвТсКК
рЊшЙ

сККНжЁЫбД
1. Construct
a fully-labelled Born-Haber cycle for the formation of MgO and use the data
given below to calculate a value for the enthalpy of lattice formation of this
oxide.
(ЈЇрЂеТЙЧбЏЈбЁУЂЭЇКЭЙ ЮвУьрКЭУьсККрЕчС ЂЭЇЁвУрЁдД MgO тДТуЊщЂщЭСйХЗешЁгЫЙДуЫщЕшЭфЛЙещ)
Process H0 , kJ
mol–1
Mg(s) + O2(g) → MgO(s) –602
Mg(s) → Mg(g) +148
Mg(g) → Mg+(g) + e– +738
Mg+(g) → Mg2+(g) + e– +1451
O2(g) → 2O(g) +498
O(g) + e– → O–(g) –141
O–(g) +
e– → O2–(g) +798
2.
A Born–Haber cycle for the formation of calcium
sulphide is shown below. The cycle includes
enthalpy changes for all Steps except Step F. (The cycle is not
drawn to scale.)
(ЧбЏЈбЁУЂЭЇКЭЙ
ЮвУьрКЭУьсЪДЇЁвУрЁдДсЄХрЋеТС
ЋбХфПДь
рЛчЙДбЇЗешсЪДЇЭТйшДщвЙХшвЇЙещ
сЕшХаЂбщЙЕЭЙфДщ
сЪДЇЛУдСвГЄЧвСУщЭЙЗешрЛХешТЙсЛХЇрЭвфЧщсХщЧ ТЁрЧщЙЂбщЙЕЭЙ F фСшфДщсЪДЇрЭвфЧщ)

(a)
Give the full electronic arrangement of the ion S2–
(ЈЇсЪДЇЁвУЈбДЭдрХчЁЕУЭЙсККрЕчСЂЭЇ S2-
......................................................................................................................................
(b) Identify the species X formed in
Step E.
(ЈЇОдЈвУГвЧшв X уЙЂбщЙЕЭЙ E ЄзЭЭафУ)
......................................................................................................................................
(c) Suggest why Step F is an endothermic process.
(ЈЇуЫщЂщЭрЪЙЭсЙаЧшврЫЕиуДЂбщЙЕЭЙ F ЈжЇрЛчЙЁУаКЧЙЁвУДйДЄЧвСУщЭЙ)
......................................................................................................................................
......................................................................................................................................
(d) Name the enthalpy change for each of the
following steps.
(ЈЇЈЭЁЊзшЭОХбЇЇвЙЗешрЛХешТЙсЛХЇуЙсЕшХаЂбщЙЕЭЙ)
(i) Step B ...............................................................................................................
(ii) Step D ...............................................................................................................
(iii) Step F ................................................................................................................
(e) Explain why the enthalpy change for Step D is
larger than that for Step C.
(ЈЇЭИдКвТЧшврЫЕиуДОХбЇЇвЙЗешрЛХешТЙсЛХЇуЙЂбщЙЕЭЙ D ЈжЇСвЁЁЧшвЂбщЙЕЭЙ C )
(f) Use the data shown in the cycle to
calculate a value for the enthalpy change for Step F.
(ЈЇЄгЙЧГЫвОХбЇЇвЙЗешЛХешТЙсЛХЇуЙЂбщЙЕЭЙ F )
3.
The energy level diagram (Born-Haber cycle) for
caesium chloride is shown below.
(сМЙМбЇсЪДЇсМЙМбЇУаДбКОХбЇЇвЙЫУзЭ ЧбЎЈбЁУЂЭЇКЭЙ
ЮвУьрКЭУь ЂЭЇЁвУрЁдДсЄХрЋеТСЄХЭфУДьрЛчЙ
ДбЇЕшЭфЛЙещ)
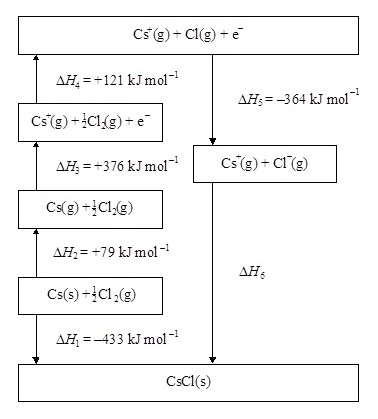
(a) Give the names of the enthalpy changes represented by ΔH1, ΔH2 and ΔH5.
(ЈЇКЭЁЊзшЭОХбЇЇвЙЂЭЇ ΔH1, ΔH2 сХа ΔH5.)
ΔH1 ...........................................................................................................................
ΔH2 ...........................................................................................................................
ΔH5 ...........................................................................................................................
(b)
Calculate the value of the lattice energy ΔH6.
(ЈЇЄгЙЧГЫвОХбЇЇвЙтЄУЇУшвЇМХжЁ ΔH6)
(c) Explain why the
enthalpy change represented by ΔH3 has a lower magnitude for caesium than
for sodium.
(ЈЇЭИдКвТЧшврЫЕиуДΔH3 ЂЭЇЋерЋеТСЈжЇЕшгЁЧшвЂЭЇтЋрДеТС)
.....................................................................................................................................
.....................................................................................................................................
.....................................................................................................................................
.....................................................................................................................................
4.
Figure 1 shows the energy level diagram (Born-Haber
cycle) for the formation of rubidium iodide from its elements.
(РвОЫСвТрХЂ 1
сЪДЇсМЙМбЇУаДбКОХбЇЇвЙЫУзЭЧбЏЈбЁУЂЭЇ
КЭЙ ЮвУьрКЭУь ЂЭЇЁвУрЁдДЪвУЛУаЁЭКУйКдрДеТСфЭтЭфДДь тДТрУдшСЕщЙЈвЁЂГаЗешрЛчЙИвЕи)
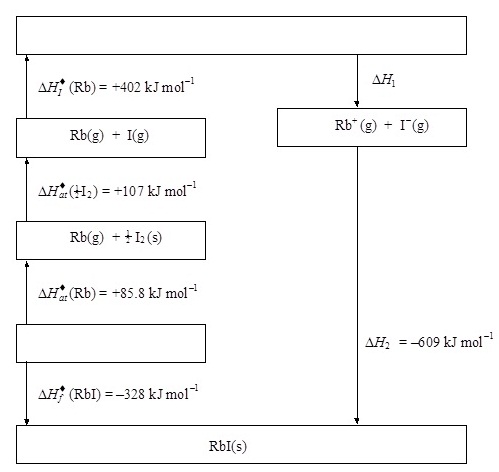
Figure 1
(i)
Complete the diagram giving the identities of the
missing species
(ЈЇЗгсМЙМбЇуЫщЪСКйУГь тДТрЕдСЪдшЇрЁдДЂжщЙуЙЊшЭЇЗешрЧщЙфЧщ)
(2)
(ii)
Give the names of the enthalpy changes represented by ΔH1 and ΔH2.
(ЈЇКЭЁЊзшЭЂЭЇОХбЇЇвЙ ΔH1 сХа ΔH2 )
ΔH1 ..................................................................................................................
ΔH2 ..................................................................................................................
(iii) Calculate the value of the enthalpy change represented
by ΔH1.
(ЈЇЄгЙЧГЧшв ΔH1 СеЄшврЗшвфУ)
5. The following data relate to lithium chloride. Standard molar
enthalpy change of
solution is –37.0 kJ
mol–1.Lattice
enthalpy is –846 kJ mol–1.
(ЂщЭСйХЕшЭфЛЙещрЛчЙЂЭЇХдрЗеТСЄХЭфУДь СеЄЧвСУщЭЙСвЕУАвЙЂЭЇЁвУХаХвТЕшЭтСХ = -37.0 kJ/mol сХаСе
ОХбЇЇвЙтЄУЇУшвЇМХжЁ
= –846 kJ mol–1. )

(i) Give the name of each of the changes A and B.
(ЈЇКЭЁЧшв A сХа
B
рЛчЙЁвУрЛХешТЙсЛХЇуД)
A...............................................
B...............................................
(ii) Calculate the value of the enthalpy change
represented by C and suggest the name(s) of the
enthalpy change(s).
(ЈЇЄгЙЧГЫвОХбЇЇвЙуЙЂбщЙ C сХаКЭЁЊзшЭЂЭЇОХбЇЇвЙДбЇЁХшвЧ)
6. (i) Draw
a fully-labelled Born–Haber cycle for the formation of solid barium chloride,
BaCl2, from its
elements10. Include state symbols for all species involved.
(ЈЇрЂеТЙсЪДЇЧбЎЈбЁУЂЭЇКЭЙ
ЮвУьрКЭУьсККрЕдС
ЂЭЇЁвУрЁдДМХжЁсКрУеТСЄХЭфУДь , BaCl2 тДТрУдшСЕщЙЈвЁ
ЂГаЗешрЛчЙИвЕи ЈЇУаКиЪЖвЙасХаЪбХбЁЩГьЂЭЇсЕшХаЂбщЙЕЭЙДщЧТ)
(ii) Use your Born–Haber cycle and the standard enthalpy data given below to
calculate a value for the electron affinity of chlorine.
(ЈЇуЊщЧбЏЈбЁУЂЭЇКЭЙ
ЮвУьрКЭУьЗешрЂеТЙЂжщЙсХаЄшвОХбЇЇвЙЕшЭфЛЙещЄгЙЧГЫвЄшвЭдрХчЁЕУЭЙЭбППдЙдЕеЂЭЇЄХЭУеЙ)
Enthalpy
of atomisation of barium +180
kJ mol–1
Enthalpy of atomisation of chlorine +122
kJ mol–1
Enthalpy of formation of barium chloride –859
kJ mol–1
First ionisation enthalpy of barium +503
kJ mol–1
Second ionisation enthalpy of barium +965
kJ mol–1
Lattice formation enthalpy of barium chloride –2056
kJ mol–1
УйЛРвОЗешрЁешТЧЂщЭЇ

Size : 2.11 KBs
Upload : 2012-11-25 09:14:40
|
|
ЕщЭЇЁвУуЫщЄасЙЙКЗЄЧвСЙещш ?
|
 
ЪЖвЙа : МйщуЊщЗбшЧфЛ
ЧдЗТвШвЪЕУь
|
|
|