ОбЙИатЄрЧрХЙЕьЗешфСшрЛчЙфЛЕвСЁЎЭЭЁрЕЕ
сСщЧшврУвЈауЊщрЫЕиМХЂЭЇЁЎЭЭЁрЕЕЭИдКвТЁвУЪУщвЇОбЙИарЄСеуЙУйЛсККЕшвЇ ц СвсХщЧ сЕшЁчОКЧшвИвЕиКвЇИвЕиЪУщвЇОбЙИатДТфСшрЛчЙфЛЕвСЁЎЭЭЁрЕЕ КвЇИвЕиСеЗбщЇЗешрЛчЙсХафСшрЛчЙфЛЕвСЁЎЭЭЁрЕЕ рЊшЙ BeCl2 BCl3 ЪбЇрЁЕ Be сХа B СерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 4 сХа 6 ЕвСХгДбК
 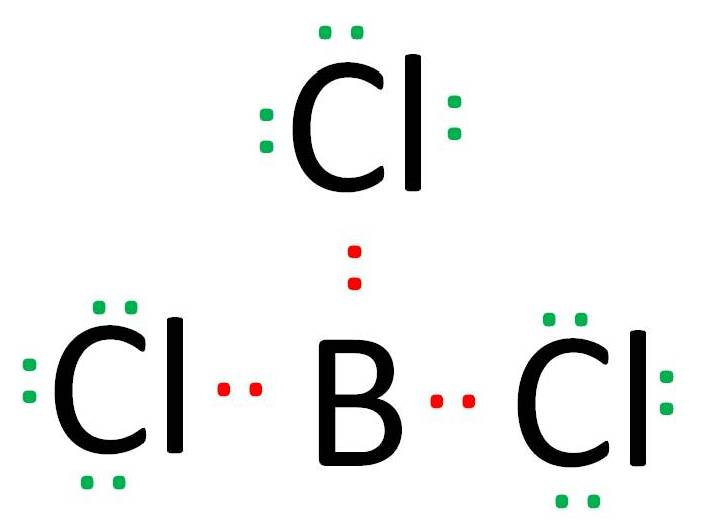
ЪдшЇЗешЙшвЪбЇрЁЕЁчЄзЭ N ЁбК P рЛчЙИвЕиЫСйш 5A рЊшЙрДеТЧЁбЙ сЕшрСзшЭрЁдДЪвУЛУаЁЭКсХщЧОКЧшвЕшвЇЁбЙ рЊшЙ рСзшЭЗгЛЏдЁдУдТвЁбК Cl ИвЕи N ЈарЁдДЪвУ NCl3 ЭТшвЇрДеТЧ ЋжшЇрЛчЙфЛЕвСЁЎЭЭЁрЕЕ уЙЂГаЗеш P ЈарЁдДЪвУ PCl3 ЋжшЇрЛчЙфЛЕвСЁЎЭЭЁрЕЕрЊшЙЁбЙ сЕшЂГарДеТЧЁбЙЈарЁдД PCl5 фДщДщЧТ сХафСшрЛчЙфЛЕвСЁЎЭЭЁрЕЕ ЄзЭуЙ PCl5 рЧрХЙЋьЭдрХчЁЕУЭЙЂЭЇ P = 10 ДбЇУйЛ
  
ЪдшЇЗшрЁдДЂжщЙЙещЭИдКвТфДщЧшв N рЛчЙИвЕиЄвКЗеш 2 ЈжЇСеУаДбКОХбЇЇвЙЪйЇЪиДЗеш n = 2 ЈжЇСеМХуЫщрЁдДфЮКУдфДрЋЊбЙфСшфДщ рОУвафСшСе subshell d ЈжЇЪУщвЇОбЙИаЁбКЭаЕЭСЭзшЙДщЧТОбЙИарДешТЧ 3 ОбЙИа ЗгуЫщСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 8 сХщЧфСшЪвСвУЖЪУщвЇОбЙИаЕшЭфЛфДщЭеЁ
сЕшЪгЫУбК P рЛчЙИвЕиЄвКЗеш 3 ЈжЇСе subshell 3d ЭТйшДщЧТ уЙРвЧаЖйЁЁУаЕищЙ ЈарЁдДфЮКУдфДрЋЊбЙ фДщфЮКУдДЭЭУьКдЗбХ sp3d ЈжЇЪУщвЇОбЙИарДешТЧЁбКЭаЕЭСЭзшЙфДщ 5 ОбЙИа ЗгуЫщСерЧрХЙЋьЭдрХчЁЕУЭЙ = 10
ЋбХрПЭУьрЛчЙЭеЁИвЕиЫЙжшЇЗешЪвСвУЖЪУщвЇОбЙИаЗбщЇрЛчЙсХафСшрЛчЙфЛЕвСЁЎЭЭЁрЕЕ рЊшЙ SF2 рЛчЙфЛЕвСЁЎЭЭЁрЕЕ сЕш SF6 фСшрЛчЙфЛЕвСЁЎЭЭЁрЕЕ


ЪгЫУбКЁъвЋСеЕУаЁйХ (ЁъвЋрЉзшЭТ) рСзшЭЭТйшуЙРвЧаЛЁЕдЈафСшЗгЛЏдЁдУдТв рОУваСерЧрХЙЋьЭдрХчЁЕУЭЙрЗшвЁбК 8 ЈбДрЕчСЗиЁЭЭУьКдЗбХЭТйшсХщЧ сЕшОКЧшврСзшЭЭТйшуЙРвЧаЖйЁЁУаЕищЙЈарЁдДфЮКУдфДрЋЊбЙ рЁдДфЮКУдДЭЭУьКдЗбХфДщЫХвТсКК тДТрЉОваЁъвЋрЉзшЭТЗешСеЭаЕЭСЂЙвДуЫш рЊшЙ Kr Xe ЗгуЫщрЁдДЪвУЛУаЁЭКфДщЫХвТЊЙдД сХаСерЧрХЙЋьЭдрХчЁЕУЭЙСвЁЁЧшв 8 рЊшЙ XeF4 XeF6

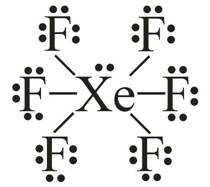
УйЛРвОЗешрЁешТЧЂщЭЇ

Size : 19.26 KBs
Upload : 2012-11-26 21:03:45
|
|
ЕщЭЇЁвУуЫщЄасЙЙКЗЄЧвСЙещш ?
|
 
ЪЖвЙа : МйщуЊщЗбшЧфЛ
ЧдЗТвШвЪЕУь
|
|
|